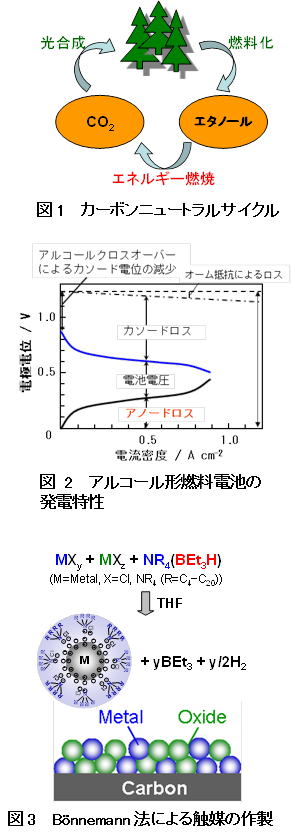
 液体アルコールを直接供給して電気を得る固体高分子形燃料電池(DAFC)は、改質ガス型(PEFC)とは異なり、燃料改質器関連機器が一切不要であるため、システム全体の構造が簡略化できます。また、起動とメンテナンスが容易となるためDAFCは産業界のみならず、車椅子用電源や携帯機器の電源としての使用が期待されています。また、アルコールの中でもエタノールは毒性が低く、バイオマスのようなカーボンニュートラルプロセス(図1)で大量に製造することができます。このため、発電時にCO2が排出されても、それが植物の光合成に使用されるためCO2の増加はゼロとみなすことができます。しかし、Pt触媒を用いた場合、アノード性能は、燃料を電気化学的に酸化する反応速度が遅いため、改質ガス形に比べて著しく低くなります(図2)。その反応速度の遅さを改善するために、PtM(M = Ru、Rh、Sn)合金やPt/RuO2、Pt/ZrO2のようなPt担持酸化物触媒が開発されてきました。中でもPtSn 触媒はエタノール酸化反応(EOR)に対する活性が高いことが報告されています。近年、Auナノ粒子と酸化物(TiO2)ナノ粒子を組み合わせた二元系金属触媒は、水性ガスシフト反応に対して高い活性を有することが報告されました。そこで、エタノール酸化に対してもPtとSnO2の両方をナノ粒子として用いることができれば、高いEOR活性が得られると考えました。本研究では、エタノールを直接供給して電気を得る固体高分子電解質形燃料電池(DEFC)用の高活性電極触媒の開発を目的として、Bonnemannらによるコロイド法を基にして作製したPt修飾SnO2ナノ粒子(Pt/SnO2)をカーボンブラック(CB)上に担持させ(以下、Pt/SnO2/CB)、そのキャラクタリゼーションおよびエタノール酸化活性を評価しました。得られました結果の一部をご紹介します。
図4(a)と1(b)にPt/SnO2(3:1)/CB触媒の異なる倍率でのTEM像を示します。図4(a)より、ナノ粒子がCB上に高分散担持されていることがわかりました。また、図4(b)より0.225 nmと0.333 nmの2種類の格子縞が観察され、それらはSnO2の(110)面(0.335 nm)とPtの(111)面(0.227nm)に帰属されました。Pt3Sn合金表面のSn原子は、酸化されてSnO2ナノ粒子を形成するため分相され、おそらくPt3Sn合金ナノ粒子の代わりにPtとSnO2がCB上に担持されたと考えられます。PtおよびSnO2ナノ粒子の平均粒径と標準偏差は、それぞれ3.1 ± 0.5 nmと2.5 ± 0.3 nmであり、両方のナノ粒子の粒径分布が狭いことがわかりました。また、Pt/CB触媒のPtナノ粒子の平均粒径は、2.4 ± 0.6 nmでありました。これらの結果は、N(Oct)4(BEt3H)が還元剤としてだけでなく、安定化剤として働いていることを示しています。
液体アルコールを直接供給して電気を得る固体高分子形燃料電池(DAFC)は、改質ガス型(PEFC)とは異なり、燃料改質器関連機器が一切不要であるため、システム全体の構造が簡略化できます。また、起動とメンテナンスが容易となるためDAFCは産業界のみならず、車椅子用電源や携帯機器の電源としての使用が期待されています。また、アルコールの中でもエタノールは毒性が低く、バイオマスのようなカーボンニュートラルプロセス(図1)で大量に製造することができます。このため、発電時にCO2が排出されても、それが植物の光合成に使用されるためCO2の増加はゼロとみなすことができます。しかし、Pt触媒を用いた場合、アノード性能は、燃料を電気化学的に酸化する反応速度が遅いため、改質ガス形に比べて著しく低くなります(図2)。その反応速度の遅さを改善するために、PtM(M = Ru、Rh、Sn)合金やPt/RuO2、Pt/ZrO2のようなPt担持酸化物触媒が開発されてきました。中でもPtSn 触媒はエタノール酸化反応(EOR)に対する活性が高いことが報告されています。近年、Auナノ粒子と酸化物(TiO2)ナノ粒子を組み合わせた二元系金属触媒は、水性ガスシフト反応に対して高い活性を有することが報告されました。そこで、エタノール酸化に対してもPtとSnO2の両方をナノ粒子として用いることができれば、高いEOR活性が得られると考えました。本研究では、エタノールを直接供給して電気を得る固体高分子電解質形燃料電池(DEFC)用の高活性電極触媒の開発を目的として、Bonnemannらによるコロイド法を基にして作製したPt修飾SnO2ナノ粒子(Pt/SnO2)をカーボンブラック(CB)上に担持させ(以下、Pt/SnO2/CB)、そのキャラクタリゼーションおよびエタノール酸化活性を評価しました。得られました結果の一部をご紹介します。
図4(a)と1(b)にPt/SnO2(3:1)/CB触媒の異なる倍率でのTEM像を示します。図4(a)より、ナノ粒子がCB上に高分散担持されていることがわかりました。また、図4(b)より0.225 nmと0.333 nmの2種類の格子縞が観察され、それらはSnO2の(110)面(0.335 nm)とPtの(111)面(0.227nm)に帰属されました。Pt3Sn合金表面のSn原子は、酸化されてSnO2ナノ粒子を形成するため分相され、おそらくPt3Sn合金ナノ粒子の代わりにPtとSnO2がCB上に担持されたと考えられます。PtおよびSnO2ナノ粒子の平均粒径と標準偏差は、それぞれ3.1 ± 0.5 nmと2.5 ± 0.3 nmであり、両方のナノ粒子の粒径分布が狭いことがわかりました。また、Pt/CB触媒のPtナノ粒子の平均粒径は、2.4 ± 0.6 nmでありました。これらの結果は、N(Oct)4(BEt3H)が還元剤としてだけでなく、安定化剤として働いていることを示しています。
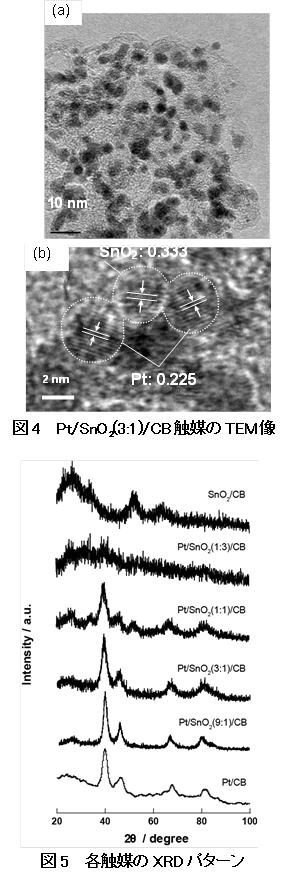 図5にPt/SnO2(9:1)/CB、Pt/SnO2(3:1)/CB、Pt/SnO2(1:1)/CB、Pt/SnO2(1:3)/CB、Pt/CB、SnO2/CB触媒のXRDパターンを示します。SnO2/CB触媒を除けば、Ptに起因するピークが認められました。Pt/SnO2(3:1)/CB触媒のPt (111)面のピークにScherrerの式を適用して求めた結晶子サイズは2.9 nmであり、この値はTEM像から求めた値とほぼ同じでありました。また、Pt/CB触媒のPtの平均粒径は、熱処理の間に1.9 nmから3.6 nmに増大しました。他方、SnO2/CB触媒のSnO2の粒径は2.0 nmでありました。これらのことから、SnO2ナノ粒子はPtの粒子成長の抑制にも効果があると推定されます。
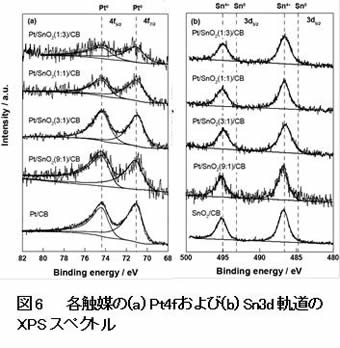
Pt/SnO2(9:1)/CB、Pt/SnO2(3:1)/CB、Pt/SnO2(1:1)/CB、Pt/SnO2(1:3)/CB、Pt/CB触媒のPt4fのXPSスペクトルを図6(a)に示します。また、Pt/SnO2(9:1)/CB、Pt/SnO2(3:1)/CB、Pt/SnO2(1:1)/CB、Pt/SnO2(1:3)/CB、SnO2/CB触媒のSn3dのXPSスペクトルを図6(b)に示します。図6(a)のPt 4fスペクトルから、PtとSnO2の組成比に関係なく触媒中のPtはすべて金属状態として存在していることがわかりました。他方、図6(b)のSn 3dスペクトルのピークは、金属状態の位置にはなく、Sn4+の位置に一致することが分かりました。この結果から触媒中のSnはSnO2として存在していることが明らかになりました。また、ピークシフトも見られないことからPtとSnは合金化していないと考えられます。さらに、XPS分析より、NやCl-のピークは見られないことから、安定化剤は全て除去されていると考えられます。
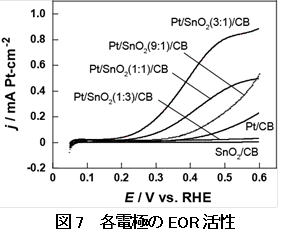
Pt/SnO2(9:1)/CB、Pt/SnO2(3:1)/CB、Pt/SnO2(1:1)/CB、Pt/SnO2(1:3)/CB、Pt/CB、SnO2/CB触媒の1 M C2H5OHを含む0.5 M H2SO4水溶液でのエタノール酸化活性を図7に示します。Pt/SnO2(9:1)/CB、Pt/SnO2(3:1)/CB、Pt/SnO2(1:1)/CB、Pt/SnO2(1:3)/CB、Pt/CB触媒において、電流密度はPtの実面積当たりで示してあります。Pt/SnO2(3:1)/CB、Pt/SnO2(1:1)/CB、Pt/SnO2(1:3)/CB 触媒は、Pt/CB触媒やSnO2/CB触媒よりも低電位でエタノール酸化が始まることがわかりました。特に、Pt/SnO2(3:1)/CB触媒を用いたときのエタノール酸化の開始電位(約0.15 V)は、Pt/CB触媒(約0.4 V)のそれと比べて約0.25 Vも負電位側にシフトすることが明らかとなりました。また、Pt/SnO2(3:1)/CB触媒の酸化電流密度は、Pt/CBのそれよりも大きいこともわかりました。これら結果は、SnO2ナノ粒子の相乗効果はエタノール酸化活性に対するPtナノ粒子の活性を向上させていることを示しています。他方、SnO2/CB触媒は、ほとんどエタノール酸化活性を示さないことがわかりました。これらの結果から、Pt/SnO2(3:1)/CBは、EORに対して、最も高い触媒活性を有していることが明らかとなりました。
エタノール電解酸化後の反応生成物を調べるために、Pt/SnO2(3:1)/CB触媒を用いて0.6 V vs. RHEで定電位電解を行いました。その結果、ガスクロマトグラフィーより電解酸化により酢酸とCO2が生成されていることがわかりました。また、酢酸およびCO2の生成量は電解酸化時間の増加とともに増加しました。3時間後の酢酸およびCO2生成の電流効率はそれぞれ約70%と約30%でありました。
図5にPt/SnO2(9:1)/CB、Pt/SnO2(3:1)/CB、Pt/SnO2(1:1)/CB、Pt/SnO2(1:3)/CB、Pt/CB、SnO2/CB触媒のXRDパターンを示します。SnO2/CB触媒を除けば、Ptに起因するピークが認められました。Pt/SnO2(3:1)/CB触媒のPt (111)面のピークにScherrerの式を適用して求めた結晶子サイズは2.9 nmであり、この値はTEM像から求めた値とほぼ同じでありました。また、Pt/CB触媒のPtの平均粒径は、熱処理の間に1.9 nmから3.6 nmに増大しました。他方、SnO2/CB触媒のSnO2の粒径は2.0 nmでありました。これらのことから、SnO2ナノ粒子はPtの粒子成長の抑制にも効果があると推定されます。
Pt/SnO2(9:1)/CB、Pt/SnO2(3:1)/CB、Pt/SnO2(1:1)/CB、Pt/SnO2(1:3)/CB、Pt/CB触媒のPt4fのXPSスペクトルを図6(a)に示します。また、Pt/SnO2(9:1)/CB、Pt/SnO2(3:1)/CB、Pt/SnO2(1:1)/CB、Pt/SnO2(1:3)/CB、SnO2/CB触媒のSn3dのXPSスペクトルを図6(b)に示します。図6(a)のPt 4fスペクトルから、PtとSnO2の組成比に関係なく触媒中のPtはすべて金属状態として存在していることがわかりました。他方、図6(b)のSn 3dスペクトルのピークは、金属状態の位置にはなく、Sn4+の位置に一致することが分かりました。この結果から触媒中のSnはSnO2として存在していることが明らかになりました。また、ピークシフトも見られないことからPtとSnは合金化していないと考えられます。さらに、XPS分析より、NやCl-のピークは見られないことから、安定化剤は全て除去されていると考えられます。
Pt/SnO2(9:1)/CB、Pt/SnO2(3:1)/CB、Pt/SnO2(1:1)/CB、Pt/SnO2(1:3)/CB、Pt/CB、SnO2/CB触媒の1 M C2H5OHを含む0.5 M H2SO4水溶液でのエタノール酸化活性を図7に示します。Pt/SnO2(9:1)/CB、Pt/SnO2(3:1)/CB、Pt/SnO2(1:1)/CB、Pt/SnO2(1:3)/CB、Pt/CB触媒において、電流密度はPtの実面積当たりで示してあります。Pt/SnO2(3:1)/CB、Pt/SnO2(1:1)/CB、Pt/SnO2(1:3)/CB 触媒は、Pt/CB触媒やSnO2/CB触媒よりも低電位でエタノール酸化が始まることがわかりました。特に、Pt/SnO2(3:1)/CB触媒を用いたときのエタノール酸化の開始電位(約0.15 V)は、Pt/CB触媒(約0.4 V)のそれと比べて約0.25 Vも負電位側にシフトすることが明らかとなりました。また、Pt/SnO2(3:1)/CB触媒の酸化電流密度は、Pt/CBのそれよりも大きいこともわかりました。これら結果は、SnO2ナノ粒子の相乗効果はエタノール酸化活性に対するPtナノ粒子の活性を向上させていることを示しています。他方、SnO2/CB触媒は、ほとんどエタノール酸化活性を示さないことがわかりました。これらの結果から、Pt/SnO2(3:1)/CBは、EORに対して、最も高い触媒活性を有していることが明らかとなりました。
エタノール電解酸化後の反応生成物を調べるために、Pt/SnO2(3:1)/CB触媒を用いて0.6 V vs. RHEで定電位電解を行いました。その結果、ガスクロマトグラフィーより電解酸化により酢酸とCO2が生成されていることがわかりました。また、酢酸およびCO2の生成量は電解酸化時間の増加とともに増加しました。3時間後の酢酸およびCO2生成の電流効率はそれぞれ約70%と約30%でありました。